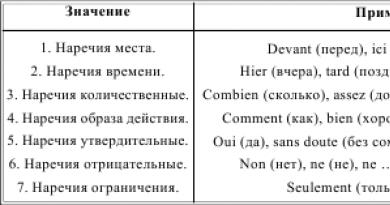
Чумна́я па́лочка (лат. Yersinia pestis ) - вид грамотрицательных бактерий из семейства энтеробактерий. Инфекционный агент бубонной чумы, также может вызывать чумную пневмонию и септическую чуму. Все три формы ответственны за высокий уровень смертности в эпидемиях, имевших место в истории человечества, например таких как «Юстинианова чума» (100 миллионов жертв) и «Чёрная смерть», на которой - смерть трети населения Европы за промежуток с 1347 по 1353 годы.
Роль Yersinia pestis в «Чёрной смерти» дискутируется. Некоторые утверждают, что «Чёрная смерть» распространилась слишком быстро, чтобы быть вызванной Yersinia pestis . ДНК этой бактерии найдены в зубах умерших от «Чёрной смерти», тогда как тестирование средневековых останков людей, умерших по другим причинам, не дало положительной реакции на Yersinia pestis . Это доказывает, что Yersinia pestis является как минимум сопутствующим фактором в некоторых (возможно, не во всех) европейских эпидемиях чумы. Возможно, что устроенный чумой отбор мог повлиять на патогенность бактерии, отсеяв индивидуумов, которые были наиболее ей подвержены.
Род Yersinia - грамотрицательные, биполярные коккобациллы. Так же, как и другие представители Enterobacteriaceae , они обладают ферментативным метаболизмом. Y. pestis производит антифагоцитарную слизь. Подвижная в культуре бактерия становится неподвижной, попав в организм млекопитающего.
История
Y. pestis была открыта в 1894 году швейцарско-французским медиком и бактериологом Пастеровского института Александром Йерсеном во время эпидемии чумы в Гонконге. Йерсен был сторонником школы Пастера. Прошедший подготовку в Германии японский бактериолог Китасато Сибасабуро, практиковавший метод Коха, также в это время был привлечён к поискам агента, являющегося возбудителем чумы. Однако именно Йерсен фактически связал чуму с Y. pestis . Долгое время возбудителя чумы относили к роду Bacterium , позже - к роду Pasteurella . В 1967 году род бактерий, к которому относился возбудитель чумы, был переименован в честь Александра Йерсена.
В результате сравнения древних штаммов генов Yersinia pestis и её вероятного предка Yersinia pseudotuberculosis (псевдотуберкулезная палочка) было выявлено, что Yersinia pestis мутировала из сравнительно безвредного микроорганизма около 10 тысяч лет назад. Выяснилось, что обитающая в почве Y. pseudotuberculosis , вызывающая легкое заболевание желудочно-кишечного тракта, приобрела тогда несколько генов, позволивших ей проникать в легкие человека. Далее, в ключевом гене Pla произошла замена одной аминокислоты, в результате чего микроорганизм смог с повышенной силой разлагать белковые молекулы в легких и размножаться по всему организму через лимфатическую систему. Исследователи подозревают, что ген Pla чумная палочка позаимствовала у другого микроба в результате горизонтального обмена генами. Это подтверждают и исследования датских и британских ученых, которые провели исследования молекул ДНК, извлеченных из зубов 101 человека бронзового века, обнаруженных на территории Евразии (от Польши до Сибири). Следы бактерии Y. pestis нашли в ДНК семерых, возрастом до 5783 лет, при этом в шести из этих образцов отсутствовали «ген вирулентности» ymt и мутации в «гене активации» pla. В дальнейшем, на рубеже второго и первого тысячелетия до нашей эры, из-за демографических условий, выразившихся в увеличении плотности населения, возникла более летальная «бубонная» мутация бактерии.
Известны три биовара бактерии; полагают, что каждый соответствует одной из исторических пандемий чумы. Биовар antiqua считают ответственным за Юстинианову чуму. Неизвестно, был ли этот биовар причиной более ранних, меньших эпидемий, или же эти случаи вообще не были эпидемиями чумы. Биовар medievalis полагают связанным с «Чёрной смертью». Биовар orientalis связывают с Третьей пандемией и большинством современных вспышек чумы.
Патогенность и иммунитет
Патогенность Yersinia pestis заключается в двух антифагоцитарных антигенах, называемых F1 и VW , оба существенны для вирулентности. Эти антигены производятся бактерией при температуре 37 °C. Кроме этого, Y. pestis выживает и производит F1 и VW антигены внутри кровяных клеток, таких, например, как моноциты, исключением являются полиморфно-ядерные нейтрофильные гранулоциты.
Некоторое время назад в США инактивированная формалином вакцина была доступна для взрослых, находящихся под большим риском заражения, однако затем продажи были прекращены по указанию FDA, специального агентства министерства здравоохранения США, по причине низкой эффективности и вероятности серьёзного воспаления. Ведутся перспективные эксперименты в генной инженерии по созданию вакцины, основанной на антигенах F1 и VW, хотя бактерии не имеющие антигена F1 сохраняют достаточную вирулентность, а антигены V достаточно изменчивы, так что вакцинация, основанная на этих антигенах может не давать достаточно полной защиты.
В России доступна живая вакцина на основе невирулентного штамма чумы.
Вакцинация не защищает от легочной чумы. Во время эпидемии 1910-1911 года применение прочумных сывороток (лимфы Хавкина и сыворотки Йерсена) лишь продлевало течение болезни на несколько дней, но не спасло жизнь ни одному больному. Впоследствии ученым окончательно стало ясно, что гуморальный иммунитет при аэрогенном инфицировании возбудителем чумы значения не имеет.
Геном
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis), штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США), штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 парных оснований, в штамме CO92 - 4 653 728 парных оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica , бактерия Y. pestis содержит плазмиды pCD1 . Вдобавок, она также содержит плазмиды pPCP1 и pMT1 , которых нет у других видов рода Yersinia . Перечисленные плазмиды и остров патогенности, названный HPI , кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов.
Лечение
С 1947 года традиционным средством первого этапа лечения от Y. pestis были стрептомицин, хлорамфеникол или тетрациклин. Также есть свидетельства положительного результата от использования доксициклина или гентамицина.
Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
Роль Yersinia pestis в «Чёрной смерти» дискутируется. Некоторые утверждают, что «Чёрная смерть» распространилась слишком быстро, чтобы быть вызванной Yersinia pestis . ДНК этой бактерии найдены в зубах умерших от «Чёрной смерти», тогда как тестирование средневековых останков людей, умерших по другим причинам, не дало положительной реакции на Yersinia pestis . Это доказывает, что Yersinia pestis является как минимум сопутствующим фактором в некоторых (возможно, не во всех) европейских эпидемиях чумы. Возможно, что устроенный чумой отбор мог повлиять на патогенность бактерии, отсеяв индивидуумов, которые были наиболее ей подвержены.
В России доступна живая вакцина на основе невирулентного штамма чумы .
Геном
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis) , штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США) , штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 парных оснований, в штамме CO92 - 4 653 728 парных оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica , бактерия Y. pestis содержит плазмиды pCD1 . Вдобавок, она также содержит плазмиды pPCP1 и pMT1 , которых нет у других видов рода Yersinia . Перечисленные плазмиды и остров патогенности , названный HPI , кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов.
Лечение
С 1947 года традиционным средством первого этапа лечения от Y. pestis были стрептомицин , хлорамфеникол или тетрациклин . Также есть свидетельства положительного результата от использования доксициклина или гентамицина .
Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
Напишите отзыв о статье "Чумная палочка"
Примечания
- Collins FM. Pasteurella, Yersinia, and Francisella. In: Barron"s Medical Microbiology (Barron S et al, eds.). - 4th ed.. - Univ of Texas Medical Branch, 1996. - ISBN .
- - в статье, напечатанной в журнале «Знание-Сила» № 2 за 2002 год приводятся размышления, критикующие связь бактерии с чумой.
- Drancourt M; Aboudharam G; Signolidagger M; Dutourdagger O; Raoult D. (1998). «». PNAS 95 (21): 12637–12640.
- Drancourt M; Raoult D. (2002). «». Microbes Infect. 4 : 105–9.
- . Lenta.ru . Проверено 23-10=2015.
- Daniel L. Zimbler, Jay A. Schroeder, Justin L. Eddy & Wyndham W. Lathem. . nature.com . Проверено 13-02=2016.
- . Lenta.ru . Проверено 23-10=2015.
- Simon Rasmussen. . cell.com. Проверено 13-02=2016.
- Salyers AA, Whitt DD. Bacterial Pathogenesis: A Molecular Approach. - 2nd ed.. - ASM Press, 2002. - ISBN pp207-12.
- Welkos S et al. . (2002). «». Vaccine 20 : 2206–2214.
- title=Вакцина чумная живая сухая (Vaccine plague) | url=http://www.epidemiolog.ru/catalog_vac/index.php?SECTION_ID=&ELEMENT_ID=476
- Супотницкий М. В. , Супотницкая Н. С., 2006 ,
- Супотницкий М. В. , Супотницкая Н. С., 2006 ,
- Deng W et al. . (2002). «». Journal of Bacteriology 184 (16): 4601–4611.
- Parkhill J et al. . (2001). «». Nature 413 : 523–527.
- Wagle PM. (1948). «Recent advances in the treatment of bubonic plague». Indian J Med Sci 2 : 489–94.
- Meyer KF. (1950). «Modern therapy of plague». JAMA 144 : 982–5.
- Kilonzo BS, Makundi RH, Mbise TJ. (1992). «A decade of plague epidemiology and control in the Western Usambara mountains, north-east Tanzania». Acta Tropica 50 : 323–9.
- Mwengee W, Butler T, Mgema S, et al. (2006). «Treatment of plague with gentamicin or doxycycline in a randomized clinical trial in Tanzania». Clin Infect Dis 42 : 614–21.
Более половины населения Европы в Средние века (XIV век) выкосила чума, известная как черная смерть. Ужас этих эпидемий остался в памяти людей по прошествии нескольких веков и даже запечатлен в полотнах художников. Далее чума неоднократно посещала Европу и уносила человеческие жизни, пусть и не в таких количествах.
В настоящее время заболевание чума остается . Около 2 тыс. человек заражается ежегодно. Из них большая часть умирает. Большинство случаев заражения отмечается в северных регионах Китая и странах Центральной Азии. По мнению специалистов для появления черной смерти сегодня нет причин и условий.
Возбудитель чумы был открыт в 1894 году. Изучая эпидемии заболевания, русские ученые разработали принципы развития заболевания, его диагностику и лечение, была создана противочумная вакцина.
Симптомы чумы зависят от формы заболевания. При поражении легких больные становятся высокозаразными, так как инфекция распространяется в окружающую среду воздушно-капельным путем. При бубонной форме чумы больные малозаразны или не заразны вовсе. В выделениях пораженных лимфоузлов возбудители отсутствуют, либо их совсем мало.
Лечение чумы стало значительно эффективнее с появлением современных антибактериальных препаратов. Смертность от чумы с этого времени снизилась до 70%.
Профилактика чумы включает в себя целый ряд мероприятий, ограничивающих распространение инфекции.
Чума является острым инфекционным зоонозным трансмиссивным заболеванием, которое в странах СНГ вместе с такими заболеваниями, как холера, туляремия и натуральная оспа считается (ООИ).
Рис. 1. Картина «Триумф смерти». Питер Брейгель.
Возбудитель чумы
В 1878 г. Г. Н. Минх и в 1894 г. А. Йерсен и Ш. Китазато, независимо друг от друга открыли возбудитель чумы. Впоследствии русские ученые изучили механизм развития заболевания, принципы диагностики и лечения, создали противочумную вакцину.
- Возбудитель заболевания (Yersinia pestis) представляет собой биполярную неподвижную коккобациллу, которая имеет нежную капсулу и никогда не образует спор. Способность образовывать капсулу и антифагоцитарную слизь не позволяет макрофагам и лейкоцитам активно бороться с возбудителем, в результате чего он быстро размножается в органах и тканях человека и животного, распространяясь с током крови и по лимфатическим путям по всему организму.
- Возбудители чумы выделяют экзотоксины и эндотоксины. Экзо- и эндотоксины содержаться в телах и капсулах бактерий.
- Ферменты агрессии бактерий (гиалуронидаза, коагулаза, фибринолизин, гемолизин) облегчают их проникновение в организм. Палочка способна проникать даже через неповрежденные кожные покровы.
- В грунте чумная палочка не теряет свою жизнеспособность до нескольких месяцев. В трупах животных и грызунов выживает до одного месяца.
- Бактерии устойчивы к низким температурам и замораживанию.
- Возбудители чумы чувствительны к высоким температурам, кислой реакции среды и солнечным лучам, которые убивают их только за 2 — 3 часа.
- До 30 дней возбудители сохраняются в гное, до 3 месяцев — в молоке, до 50 дней — в воде.
- Дезинфицирующие вещества уничтожают чумную палочку за несколько минут.
- Возбудители чумы вызывают заболевание у 250 видов животных. Среди них составляют большинство грызуны. Подвержены заболеванию верблюды, лисицы, кошки и другие животные.

Рис. 2. На фото чумная палочка — бактерия, вызывающая чуму — Yersinia pestis.
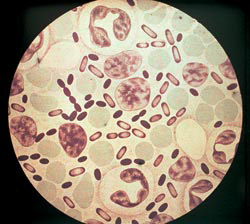
Рис. 3. На фото возбудители чумы. Интенсивность окраски анилиновыми красителями наибольшая на полюсах бактерий.
Php?post=4145&action=edit#
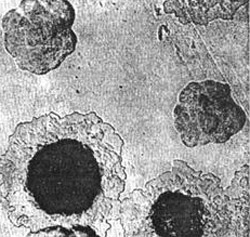
Рис. 4. На фото возбудители чумы — рост на плотной среде колонии. Вначале колонии похожи на битое стекло. Далее их центральная часть уплотняется, а периферия напоминает кружева.
Эпидемиология
Резервуар инфекции
Легко восприимчивы к чумной палочке грызуны (тарбаганы, сурки, песчанки, суслики, крысы и домовые мыши) и животные (верблюды, кошки, лисицы, зайцы, ежи и др). Из лабораторных животных подвержены инфекции белые мыши, морские свинки, кролики и обезьяны.
Собаки никогда не болеют чумой, но передают возбудитель через укусы кровососущих насекомых — блох. Погибшее от заболевания животное перестает быть источником инфекции. Если грызуны, инфицированные чумными палочками, впали в спячку, то заболевание у них приобретает латентное течение, а после спячки они вновь становятся распространителями возбудителей. Всего насчитывается до 250 видов животных, которые болеют, а значит являются источником и резервуаром инфекции.

Рис. 5. Грызуны — резервуар и источник возбудителя чумы.
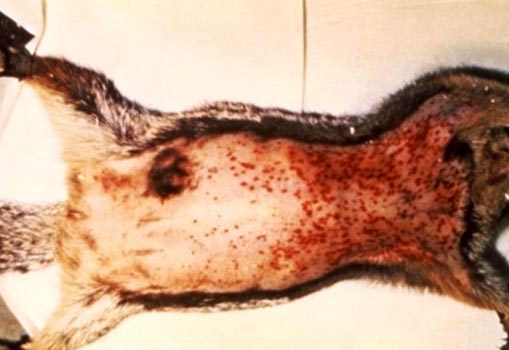
Рис. 6. На фото признаки чумы у грызунов: увеличенные лимфоузлы и множественные кровоизлияния под кожей.

Рис. 7. На фото малый тушканчик — переносчик заболевания чумой в Средней Азии.

Рис. 8. На фото черная крыса — переносчик не только чумы, но и лептоспироза, лейшманиоза, сальмонеллеза, трихинеллеза и др.
Пути заражения
- Основной путь передачи возбудителей — через укусы блох (трансмиссивный путь).
- Инфекция может попасть в организм человека при работе с больными животными: убой, снятие и разделка шкуры (контактный путь).
- Возбудители могут попасть в организм человека с зараженными продуктами питания, в результате их недостаточной термической обработки.
- От больного с легочной формой чумы инфекция распространяется воздушно-капельным путем.

Рис. 9. На фото блоха на коже человека.

Рис. 10. На фото момент укуса блохи.
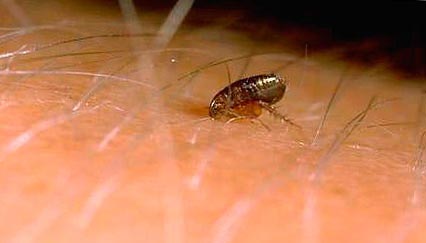
Рис. 11. Момент укуса блохи.
Переносчики возбудителя
- Переносчиками возбудителей являются блохи (в природе существует более 100 видов этих членистоногих насекомых),
- Переносчиками возбудителей являются некоторые виды клещей.

Рис. 12. На фото блоха – основной переносчик чумы. В природе существует более 100 видов этих насекомых.

Рис. 13. На фото сусликовая блоха – основной переносчик чумы.
Как происходит заражение
Заражение происходит через укус насекомого и втирание его фекалий и содержимого кишечника при срыгивании в процессе питания. При размножении бактерий в кишечной трубке блохи под воздействием коагулазы (фермента, выделяемого возбудителями) образуется «пробка», которая препятствует поступлению крови человека в ее организм. В результате чего блоха срыгивает сгусток на кожные покровы укушенного. Инфицированные блохи остаются высокозаразными в течение от 7 недель и до 1 года.

Рис. 14. На фото вид укуса блохи – пуликозное раздражение.

Рис. 15. На фото характерная серия укусов блохи.
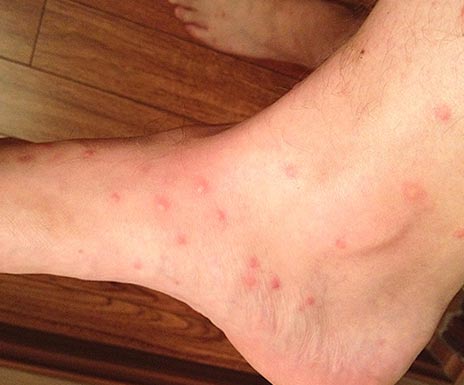
Рис. 16. Вид голени при укусах блох.

Рис. 17. Вид бедра при укусах блох.
Человек, как источник инфекции
- При поражении легких больные становятся высокозаразными. Инфекция распространяется в окружающую среду воздушно-капельным путем.
- При бубонной форме чумы больные малозаразны или не заразны вовсе. В выделениях пораженных лимфоузлов возбудители отсутствуют, либо их совсем мало.
Механизмы развития чумы
Способность чумной палочки образовывать капсулу и антифагоцитарную слизь не позволяет макрофагам и лейкоцитам активно с ней бороться, в результате чего возбудитель быстро размножается в органах и тканях человека и животного.
- Возбудители чумы через поврежденные кожные покровы и далее по лимфатическим путям проникают в лимфатические узлы, которые воспаляются и образуют конгломераты, (бубоны). На месте укуса насекомого развивается воспаление.
- Проникновение возбудителя в кровяное русло и его массивное размножение приводит к развитию бактериального сепсиса.
- От больного с легочной формой чумы инфекция распространяется воздушно-капельным путем. Бактерии попадают в альвеолы и вызывают тяжелую пневмонию.
- В ответ на массивное размножение бактерий организм больного вырабатывает огромное число медиаторов воспаления. Развивается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), при котором поражаются все внутренние органы. Особую опасность для организма представляют кровоизлияния в мышцу сердца и надпочечники. Развившийся инфекционно-токсический шок становится причиной гибели больного.
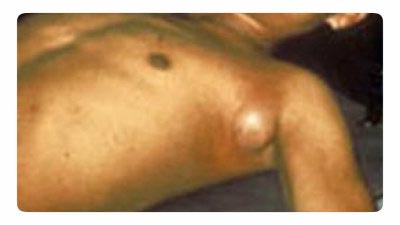
Рис. 18. На фото бубонная чума. Типичное увеличение лимфатического узла в подмышечной зоне.
Симптомы чумы
Болезнь проявляется после проникновения возбудителя в организм на 3 – 6 сутки (редко, но отмечены случаи проявления заболевания на 9 сутки). При попадании инфекции в кровь инкубационный период составляет несколько часов.
Клиническая картина начального периода
- Острое начало, большие цифры температуры и ознобы.
- Миалгии (мышечные боли).
- Мучительная жажда.
- Сильное проявление слабости.
- Быстрое развитие психомоторного возбуждения («очумелыми» называют таких больных). На лице появляется маска ужаса («маска чумы»). Реже отмечается заторможенность и апатия.
- Лицо становится гиперемированным и одутловатым.
- Язык густо обложен белым налетом («меловой язык»).
- На коже появляются множественные геморрагии.
- Значительно учащается сердечный ритм. Появляется аритмия. Падает артериальное давление.
- Дыхание становится поверхностным и учащенным (тахипноэ).
- Количество выделяемой мочи резко снижается. Развивается анурия (полное отсутствие выделения мочи).
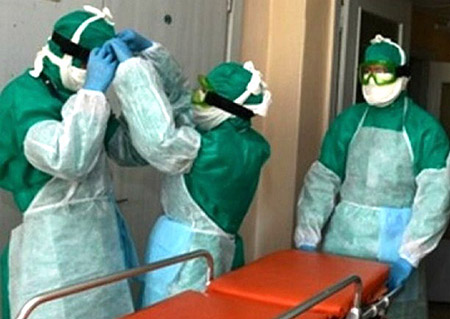
Рис. 19. На фото помощь больному чумой оказывается медиками, одетыми в противочумные костюмы.
Формы заболевания чумой
Локальные формы заболевания
Кожная форма
На месте укуса блохи или контакта с инфицированным животным на кожных покровах появляется папула, которая быстро изъязвляется. Далее появляется черный струп и рубец. Чаще всего кожные проявления являются первыми признаками более грозных проявлений чумы.
Бубонная форма
Самая частая форма проявления заболевания. Увеличение лимфоузлов проявляется вблизи места укуса насекомого (паховые, подмышечные, шейные). Чаще воспаляется один лимфоузел, реже – несколько. При воспалении сразу нескольких лимфоузлов образуется болезненный бубон. Вначале лимфоузел твердой консистенции, болезненный при пальпации. Постепенно он размягчается, приобретая тестообразную консистенцию. Далее лимфоузел либо рассасывается, либо изъязвляется и склерозируется. Из пораженного лимфатического узла инфекция может попасть в кровяное русло, с последующим развитием бактериального сепсиса. Острая фаза бубонной формы чумы длится около недели.

Рис. 20. На фото пораженные шейные лимфоузлы (бубоны). Множественные кровоизлияния кожных покровов.
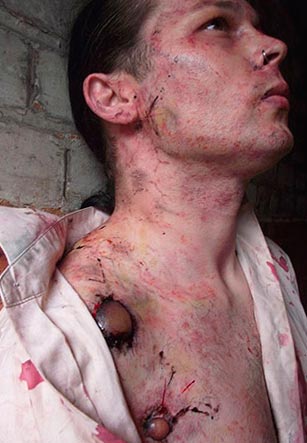
Рис. 21. На фото бубонная форма чумы — поражение шейных лимфоузлов. Множественные кровоизлияния в кожных покровах.

Рис. 22. На фото бубонная форма чумы.
Распространенные (генерализованные) формы
При попадании возбудителя в кровяное русло развиваются распространенные (генерализованные) формы чумы.
Первично-септическая форма
Если инфекция, минуя лимфоузлы, сразу попадает в кровь, то развивается первично-септическая форма заболевания. Молниеносно развивается интоксикация. При массивном размножении возбудителей в организме больного вырабатывается огромное число медиаторов воспаления. Это приводит к развитию синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдром), при котором поражаются все внутренние органы. Особую опасность для организма представляют кровоизлияния в мышцу сердца и надпочечники. Развившийся инфекционно-токсический шок становится причиной гибели больного.
Вторично-септическая форма заболевания
При распространении инфекции за пределы пораженных лимфоузлов и попадании возбудителей заболевания в кровяное русло развивается инфекционный сепсис, что проявляется резким ухудшением состояния больного, усилением симптомов интоксикации и развитием ДВС-синдрома. Развившийся инфекционно-токсический шок становится причиной гибели больного.

Рис. 23. На фото септическая форма чумы — последствия ДВС-синдрома.

Рис. 24. На фото септическая форма чумы — последствия ДВС-синдрома.
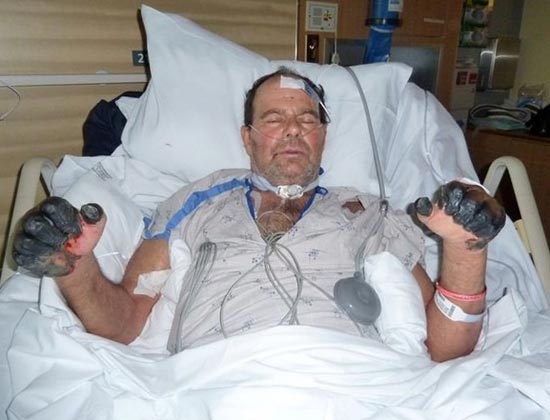
Рис. 25. 59-летний Пол Гэйлорд (житель города Портленд, штат Орегон, США). Бактерии чумы попали в его организм от бродячей кошки. В результате развившейся вторично-септической формы заболевания ему были ампутированы пальцы на руках и ногах.

Рис. 26. Последствия ДВС-синдрома.
Внешнедиссеминированные формы заболевания
Первично-легочная форма
Легочная форма чумы является самой тяжелой и опасной формой заболевания. Инфекция проникает в альвеолы воздушно-капельным путем. Поражение легочной ткани сопровождается кашлем и одышкой. Повышение температуры тела протекает с сильными ознобами. Мокрота вначале заболевания густая и прозрачная (стекловидная), потом становится жидкой и пенистой, с примесью крови. Скудные данные физикальных исследований не соответствуют тяжести заболевания. Развивается ДВС-синдром. Поражаются внутренние органы. Особую опасность для организма представляют кровоизлияния в сердечную мышцу и надпочечники. Смерть больного наступает от инфекционно-токсического шока.
При поражении легких больные становятся высокозаразными. Они формируют вокруг себя очаг особо опасного инфекционного заболевания.
Вторично-легочная форма
Является крайне опасной и тяжелой формой заболевания. Возбудители проникают в легочную ткань из пораженных лимфоузлов или с током крови при бактериальном сепсисе. Клиника и исход заболевания, как при первично-легочной форме.
Кишечная форма
Существование данной формы заболевания считается спорным. Предполагается, что заражение возникает с употреблением инфицированных продуктов. Вначале на фоне интоксикационного синдрома появляются боли в животе и рвота. Далее присоединяется понос и многочисленные позывы (тенезмы). Стул обильный слизисто-кровянистый.
Рис. 27. Фото противочумного костюма — особая экипировка медицинских работников при ликвидации очага особо опасного инфекционного заболевания.
Лабораторная диагностика чумы
Основой диагностики чумы является быстрое обнаружение чумной палочки. Вначале проводится бактериоскопия мазков. Далее выделяется культура возбудителя, которой заражаются подопытные животные.
Материалом для исследования служит содержимое бубона, мокрота, кровь, кал, кусочки ткани органов умерших и трупов животных.
Бактериоскопия
Возбудителем чумы (Yersinia pestis) является палочковидная биполярная коккобацилла. Анализ на обнаружение чумной палочки методом прямой бактериоскопии является наиболее простым и быстрым способом. Время ожидания результата составляет не более 2-х часов.
Посевы биологического материала
Культура возбудителя чумы выделяется в специализированных режимных лабораториях, предназначенных для работы с . Время роста культуры возбудителя составляет двое суток. Далее проводится тест на чувствительность к антибиотикам.
Серологические методы
Применение серологических методов позволяет определить наличие и рост антител в сыворотке крови больного к возбудителю чумы. Время получения результата составляет 7 дней.

Рис. 28. Диагностика чумы проводится в специальных режимных лабораториях.
Рис. 29. На фото возбудители чумы. Флюоросцентная микроскопия.

Рис. 30. На фото культура Yersinia pestis.
Иммунитет при чуме
Антитела на внедрение возбудителя чумы образуются в достаточно поздние сроки развития заболевания. Иммунитет после перенесенного заболевания не длительный и не напряженный. Отмечаются повторные случаи заболевания, которые протекают так же тяжело, как и первые.
Лечение чумы
До начала лечения больной госпитализируется в отдельный бокс. Медицинский персонал, обслуживающий больного, одевается в специальный противочумный костюм.
Антибактериальное лечение
Антибактериальное лечение начинается при первых признаках и проявлениях заболевания. Из антибиотиков предпочтение отдается антибактериальным препаратам группы аминогликозидов (стрептомицин), группы тетрациклинов (вибромицин, морфоциклин), группы фторхинолонов (ципрофлоксацин), группы ансамицинов (рифампицин). Хорошо зарекомендовал себя при лечении кожной формы заболевания антибиотик группы амфениколов (кортримоксазол). При септических формах заболевания рекомендуется комбинация антибиотиков. Курс антибактериальной терапии составляет не менее 7 – 10 дней.
Лечение, направленное на разные этапы развития патологического процесса
Цель патогенетической терапии – снизить интоксикационный синдром путем выведения токсинов из крови больного.
- Показано введение свежезамороженной плазмы, белковых препаратов, реополиглюкина и других препаратов в сочетании с форсированным диурезом.
- Улучшение микроциркуляции достигается при применении трентала в сочетании с салкосерилом или пикамилоном.
- При развитии геморрагий немедленно проводится плазма-ферез с целью купирования синдрома диссеминированного внутрисосудистого свертывания.
- При падении давления назначается допамид. Это состояние говорит о генерализации и развитии сепсиса.
Симптоматическое лечение
Симптоматическое лечение нацелено на подавление и устранение проявлений (симптомов) чумы и, как следствие, облегчение страданий больного. Оно направлено на устранение боли, кашля, одышки, удушья, тахикардии и др.
Больной считается здоровым, если исчезли все симптомы заболевания и получено 3 отрицательных результата бактериологического исследования.
Противоэпидемические мероприятия
Выявление больного чумой является сигналом к незамедлительному проведению , которые включают в себя:
- проведение карантинных мероприятий;
- немедленная изоляция больного и проведение профилактического антибактериального лечения обслуживающего персонала;
- дезинфекция в очаге возникновения заболевания;
- вакцинация лиц, контактирующих с больным.
После прививки противочумной вакциной иммунитет сохраняется в течение года. Повторно прививаются через 6 мес. лица, которым угрожает повторное заражение: пастухи, охотники, работники сельского хозяйства и сотрудники противочумных учреждений.

Рис. 31. На фото бригада медиков одета в противочумные костюмы.
Прогноз заболевания
Прогноз заболевания чумой зависит от следующих факторов:
- формы заболевания,
- своевременности начатого лечения,
- наличия всего арсенала медикаментозного и немедикаментозного видов лечения.
Наиболее благоприятный прогноз у больных с поражением лимфоузлов. Смертность при этой форме заболевания достигает 5%. При септической форме заболевания показатель смертности достигает 95%.
Чума является и даже при применении всех необходимых лекарственных препаратов и манипуляций болезнь зачастую заканчивается смертью больного. Возбудители чумы постоянно циркулирует в природе и не поддается полному уничтожению и контролю. Симптомы чумы разнообразны и зависят от формы заболевания. Бубонная форма чумы является самой распространенной.
Статьи раздела "Особо опасные инфекции" Самое популярное
Чума (pestis) - это острое инфекционное заболевание, проявляющееся общей интоксикацией и характерными воспалительными процессами в лимфатических узлах, легких, коже и других органах. Чума относится к группе так называемых особо опасных (карантинных) инфекций с . В СССР ликвидирована.
Этиология . Возбудитель - чумная палочка с закругленными концами, вздутая в середине, вследствие чего имеет овоидную форму. Красится обычными анилиновыми красками; средняя часть окрашивается бледнее (биполярная окраска). Устойчивость к воздействию внешней среды невелика. Высушивание, солнечный свет, конкуренция гнилостных микробов быстро ее губят; кипячение убивает в течение 1 мин. Низкую температуру палочка переносит хорошо. Микроб может выживать долго на белье, одежде, загрязненных мокротой, гноем, кровью; длительно сохраняется в воде, на пищевых продуктах. В трупах грызунов, если не наступает процесс гниения (зимой), палочка может сохранять жизнеспособность в течение 4-5 мес. Растворы 5% лизола и 5-10% карболовой кислоты убивают палочку чумы за 5-10 мин., а раствор сулемы 1: 1000 за 1-2 мин.
Эпидемиология . Хранителем инфекции в природе являются дико-обитающие грызуны (суслики, сурки, песчанки). Достаточная плотность и непрерывность колоний грызунов, большая численность блох - инфекции, способность зимоспящих сусликов и сурков переносить инфекцию в латентной форме обеспечивают непрерывную циркуляцию возбудителя чумы среди этих грызунов. К чуме весьма восприимчивы и домашние крысы, домовые мыши, обыкновенные полевки, степные пеструшки и другие мышевидные. Бесконечно длительное хранение возбудителя чумы в природе эти грызуны обеспечить не могут. Но это не исключает возможности возникновения мощных (см.) среди мышевидных, особенно при так называемых мышиных напастях, что в свою очередь влечет за собой тяжелую среди людей. Для поддержания длительно протекающих эпизоотии среди грызунов необходима высокая плотность и большая численность блох на них. Такие условия обычно создаются лишь в южных широтах, например в странах Среднего и Дальнего Востока, где инфекция чумы среди людей распространяется обычно синантропными крысами. Серьезное значение имеет восприимчивый к чуме верблюд. В прошлом нередко отмечались вспышки чумы среди людей, связанных с вынужденным убоем больных верблюдов. Восприимчивые к чуме лисы, шакалы, хорьки не имеют большого практического значения. Инфекция среди грызунов распространяется преимущественно трансмиссивным путем (через блох).
Распространение чумы среди людей возможно трансмиссивным, воздушно-капельным и контактно-бытовым путями. Возникновение первых случаев чумы среди людей всегда начинается с бубонных форм как результат трансмиссивного или контактного механизма передачи инфекции (укус блохи, снятие шкурки с больного грызуна, разделка туши верблюда при убое больного животного и т. д.). В дальнейшем развитие заболеваний определяется и другими механизмами передачи: через инфицированные предметы обихода, и воду. Если бубонная форма чумы осложняется вторичной чумной , то больной рассеивает инфекцию при кашле, разговоре. Воздушно-капельный путь заражения влечет за собой возникновение первичных легочных форм чумы, при которых больные массивно инфицируют окружающую среду.
Патогенез и патологическая анатомия . Местом входных ворот инфекции при чуме у людей могут быть кожа, слизистая оболочка дыхательных путей, конъюнктива, реже заражение происходит через . Соответственно различают кожную форму чумы, переходящую вскоре в кожно-бубонную вследствие развития регионарного бубона. Кожная форма встречается сравнительно редко (до 3-5%). Чаще наблюдается бубонная форма чумы при которой бубон (воспаление лимфатического узла) - обязательный признак. Возбудитель чумы заносится в узел с током лимфы и вызывает воспаление. Первичные бубоны отличают от вторичных, возникающих гематогенно (через кровь) обычно позже. Гематогенно инфекция может поступать в легкие (вторичная легочная чума), головной мозг (возможен менингит), а в некоторых случаях привести к (вторичная септическая чума). При первичной легочной чуме поражение легких чаще носит очаговый характер. В тяжелых случаях воспалительный процесс захватывает целую долю или несколько долей, характерен серозно-геморрагический . Кишечная форма встречается очень редко.
Чума (pestis) - острое инфекционное заболевание из группы зоонозов, проявляющееся развитием острой интоксикации и воспалительных процессов в лимфатических узлах, легких и других органах.
В настоящее время заболевания чумой регистрируются в Азии, Африке, Северной и преимущественно Южной Америке. Европа и Австралия от чумы свободны.
Этиология
Возбудитель Ч,- Bacterium pestis, Pasteurella pestis - полиморфная палочка длиной 1-3 мк и шириной 0,3-0,7 мк. Концы бактерий закруглены, а середина слегка вздута, вследствие чего они имеют овоидную (яйцевидную) форму. Легко окрашиваются анилиновыми красками, грамотрицательны. При окраске средняя часть микробных клеток окрашивается бледнее, чем концы их (биполярная окраска), особенно при окраске метиленовым синим и по Романовскому - Гимзе (рис. 1). Бактерии овоидной формы с четко выраженной биполярной окраской преобладают в мазках из пунктатов бубона, из крови и органов свежих трупов людей и животных.
Рис. 1. Биполярно окрашенные палочки чумы из селезенки морской свинки (Х1200).
Рис. 2. Двухсуточная колония чумного микроба на агаре (Х40).
Измененные формы бактерий (шары, утолщенные нити) встречаются в мазках из нагноившихся бубонов, из органов загнивших трупов и при росте на агаре с добавлением соли. В окрашенных мазках из 24-48-часовой агаровой культуры обнаруживаются короткие палочки (кокко-типы) и палочки, расположенные поодиночке и группами. Среди них встречаются длинные извитые
нити и шарообразные (инволюционные) формы. В мазках из бульонной культуры - палочки различной длины, расположенные в виде цепочек.
Бактерии чумы не обладают активной подвижностью, спор не образуют, имеют капсулу. На искусственных питательных средах образованию капсулы способствуют выращивание при t° 37°, влажная и слегка кислая среда, добавление к среде крови, гликокола и выращивание в атмосфере, содержащей 20-25% углекислоты.
Возбудитель чумы - факультативный анаэроб. Хорошо растет на обычных питательных средах с оптимальной рН среды, равной 6,9-7,2 при t° 25-30°.
Обычно растет в R-форме, иногда в S-форме. В R-форме колонии шероховатые, выпуклые, с коричневым центром, окруженные по периферии кружевной каймой (рис. 2); в S-форме - гладкие, прозрачные, без кружевной зоны. Вирулентные чумные микробы, выделяемые от больных грызунов и людей, а также из блох, растут в R-форме.
Бактерии чумы желатину и свернутую сыворотку не разжижают; ферментируют с образованием кислоты глюкозу, мальтозу, маннит и арабинозу, не ферментируют лактозу, сахарозу и рамнозу. По отношению к глицерину различают две разновидности чумного микроба: глицеринопозитивную и глицеринонегативную.
Возбудитель чумы хорошо переносит низкую температуру, но весьма чувствителен к теплу; при t° 58° погибает в течение 30 мин., а при температуре кипения - в течение 1- 5 мин. Чувствителен к действию прямых солнечных лучей. Малоустойчив к действию дезинфицирующих веществ: 3-5% раствор карболовой кислоты, растворы лизола, хлорамина, хлорной извести, этиловый спирт убивают его в течение 1-10 мин. В белковой среде (кровавая мокрота, кровь и др.) микробы чумы, предохраненные от действия света и высыхания, могут сохраняться до 10-15 дней и более, а также более устойчивы к дезинфицирующим средствам. Длительное время (3-5 мес.) они сохраняются в организме блох. В объектах внешней среды, загрязненных другой микрофлорой, быстро погибают. Чувствительны к антибиотикам (стрептомицин, тетрациклины и др.).
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках (, и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Морфология возбудителя чумы
Yersinia pestis имеет длину 1-2 мкм и толщину 0,3-0,7 мкм. В мазках из организма больного и из трупов погибших от чумы людей и грызунов выглядит как короткая овоидная (яйцевидная) палочка с биполярной окраской. В мазках из бульонной культуры палочка располагается цепочкой, в мазках из агаровых культур - беспорядочно. Биполярная окраска в том и другом случае сохраняется, но в мазках из агаровых культур несколько слабее. Возбудитель чумы по Граму окрашивается отрицательно, лучше красится щелочными и карболовыми красителями (синькой Леффлера), спор не образует, жгутиков не имеет. Содержание Г + Ц в ДНК - 45,8-46,0 мол % (для всего рода). При температуре 37 °С образует нежную капсулу белковой природы, которая выявляется на влажных и слегка кислых питательных средах.
Биохимические свойства возбудителя чумы
Yersinia pestis - аэроб, дает хороший рост на обычных питательных средах. Оптимальная для роста температура 27-28 °С (диапазон - от 0 до 45 °С), РН = 6,9-7,1. Палочка чумы дает характерный рост на жидких и плотных питательных средах: на бульоне он проявляется образованием рыхлой пленки, от которой спускаются нити в виде сосулек, напоминающих сталактиты, на дне - рыхлый осадок, бульон остается прозрачным. Развитие колоний на плотных средах проходит через три стадии: через 10-12 часов под микроскопом рост в виде бесцветных пластинок (стадия «битого стекла»); через 18-24 часа - стадия «кружевных платочков», при микроскопировании заметна светлая кружевная зона, расположенная вокруг выступающей центральной части, желтоватой или слегка буроватой окраски. Через 40-48 часов наступает стадия «взрослой колонии» - буровато-очерченный центр с выраженной периферической зоной. Yersinia pseudotuberculosis и Yersinia enterocolitica стадии «битого стекла» не имеют. На средах с кровью колонии Yersinia pestis зернистые со слабо выраженной периферической зоной. С целью быстрейшего получения характерного для Yersinia pestis роста на средах к ним рекомендуется добавлять стимуляторы роста: сульфит натрия, кровь (или ее препараты) или лизат культуры сарцины. Палочке чумы свойствен выраженный полиморфизм, особенно на средах с повышенной концентрацией NaCl, в старых культурах, в органах разложившихся чумных трупов.
Чумная палочка не имеет оксидазы, не образует индола и H2S, обладает каталазной активностью и ферментирует глюкозу, мальтозу, галактозу, маннит с образованием кислоты без газа.
, , , , , , ,
Антигенный состав возбудителя чумы
У Yersinia pestis, Yersinia pseudotuberculosis и Yersinia enterocolitica обнаружено до 18 сходных соматических антигенов. Для Yersinia pestis характерно наличие капсульного антигена (фракция I), антигенов Т, V-W, белков плазмокоагулазы, фибринолизина, белков наружной мембраны и рНб-антигена. Однако в отличие от Yersinia pseudotuberculosis и Yersinia enterocolitica, Yersinia pestis в антигенном отношении более однородна; серологической классификации этого вида нет.
, , , , , , , ,
Резистентность возбудителя чумы
В мокроте палочка чумы может сохраняться до 10 дней; на белье и одежде, испачканных выделениями больного, сохраняется неделями (белок и слизь охраняют ее от губительного действия высыхания). В трупах людей и животных, погибших от чумы, выживает с начала осени до зимы; низкая температура, замораживание и оттаивание не убивают ее. Солнце, высыхание, высокая температура губительны для Yersinia pestis. Нагревание до 60 °С убивает через 1 час, при температуре 100 °С погибает через несколько минут; 70% спирт, 5 % раствор фенола, 5 % раствор лизола и некоторые другие химические дезинфектанты убивают за 5-10-20 минут.
Факторы патогенности возбудителя чумы
Yersinia pestis является самой патогенной и агрессивной среди бактерий , поэтому и вызывает наиболее тяжелое заболевание. У всех чувствительных к нему животных и у человека возбудитель чумы подавляет защитную функцию фагоцитарной системы. Он проникает в фагоциты, подавляет в них «окислительный взрыв» и беспрепятственно размножается. Неспособность фагоцитов осуществить свою киллерную функцию в отношении Yersinia pestis - основная причина восприимчивости к чуме. Высокая инвазивность, агрессивность, токсигенность, токсичность, аллергенность и способность подавлять фагоцитоз обусловлены наличием у У. pestis целого арсенала факторов патогенности, которые перечислены ниже.
Значительная часть факторов патогенности Yersinia pestis контролируется генами, носителями которых являются следующие 3 класса плазмид, обнаруживаемых обычно вместе у всех патогенных штаммов:
- pYP (9,5 т. п. н.) - плазмида патогенности. Несет 3 гена:
- pst - кодирует синтез пестицина;
- pim - определяет иммунитет к пестицину;
- pla - определяет фибринолитическую (активатор плазминогена) и плазмо-коагулазную активность.
- pYT (65 МД) - плазмида токсигенности. Несет гены, определяющие синтез «мышиного» токсина (сложный белок, состоящий из двух фрагментов А и В, с м. м. 240 и 120 кД соответственно), и гены, контролирующие белковый и липопротеиновый компоненты капсулы. Третий ее компонент контролирует гены хромосомы. Ранее плазмида имела название pFra.
- pYV (110 т. п. н.) - плазмида вирулентности.
Она определяет зависимость роста Y. pestis при 37 °С от присутствия в среде ионов Са2+, поэтому имеет другое название - Lcr-плазмида (англ. low calcium response). Гены этой, особенно важной, плазмиды кодируют также синтез антигенов V и W и термоиндуцируемых белков Yop. Их синтез осуществляется под сложным генетическим контролем при температуре 37 °С и в отсутствие в среде Са2+. Все типы Yop-белков, кроме YopM и YopN, гидролизуются за счет активности активатора плазминогена (ген pla плазмиды pYP). Белки Yop во многом определяют вирулентность Yersinia pestis. YopE-белок обладает антифагоцитарным и цитотоксическим действием. YopD обеспечивает проникновение YopE в клетку-мишень; YopH обладает антифагоцитарной и протеин-тирозин-фосфатазной активностью; белок YopN - свойствами кальциевого сенсора; YopM связывается с атромбином крови человека.
, , ,
Постинфекционный иммунитет
Постинфекционный иммунитет прочный, пожизненный. Повторные заболевания чумой наблюдаются крайне редко. Природа иммунитета клеточная. Хотя антитела появляются и играют определенную роль в приобретенном иммунитете, он опосредуется главным образом Т-лимфоцитами и макрофагами. У лиц, переболевших чумой или вакцинированных, фагоцитоз имеет завершенный характер. Он и обусловливает приобретенный иммунитет.
Эпидемиология чумы
Круг теплокровных носителей чумного микроба чрезвычайно обширен и включает более 200 видов 8 отрядов млекопитающих. Основным же источником чумы в природе являются грызуны и зайцеобразные. Естественная зараженность установлена у более чем 180 их видов, свыше 40 из них входят в состав Фауны России и сопредельных территорий (в пределах бывшего СССР). Из 60 видов блох, для которых в экспериментальных условиях установлена возможность переноса возбудителя чумы, на этой территории обитают 36.
Чумной микроб размножается в просвете пищеварительной трубки блох. В ее переднем отделе образуется пробка («чумной блок»), содержащая большое количество микробов. При укусе млекопитающих с обратным током крови в ранку с пробки смывается часть микробов, что и ведет к заражению. Кроме того, выделяемые блохой при питании экскременты при попадании в ранку также могут вызывать заражение.
Основные (главные) носители Y. pestis на территории России и Средней Азии - суслики, песчанки и сурки, в некоторых очагах также пищухи и полевки. С ними связано существование следующих очагов чумы.
- 5 очагов, в которых основным носителем чумного микроба выступает малый суслик (Северо-Западный Прикаспий; Терско-Сунженское междуречье; Приэльбрусский очаг; Волго-Уральский и Зауральский полупустынные очаги).
- 5 очагов, в которых носители - суслики и сурки (на Алтае - пищухи): Забайкальский, Горно-Алтайский, Тувинский и высокогорные Тянь-Шанский и Памиро-Алайский очаги.
- Волго-Уральский, Закавказский и Среднеазиатский пустынные очаги, где основные носители - песчанки.
- Высокогорные Закавказский и Гиссарский очаги с основными носителями - полевками.
Разные классификации Yersinia pestis основываются на разных группах признаков - биохимических особенностях (глицерин-позитивные и глицерин-негативные варианты), области распространения (океанические и континентальные варианты), видах основных носителей (крысиный и сусликовый варианты). По одной из наиболее распространенных классификаций, предложенной в 1951 г. французским исследователем чумы Р. Девинья (R. Devignat), в зависимости от географического распространения возбудителя и его биохимических свойств различают три внутривидовые формы (биовара) Yersinia pestis.
По классификации отечественных ученых (Саратов, 1985), вид Yersinia pestis разделен на 5 подвидов: Yersinia pestis subsp. pestis (основной подвид; он включает все три биовара классификации Р. Девинья), Y. pestis subsp. altaica (алтайский подвид), Yersinia pestis subsp. caucasica (кавказский подвид), Y. pestis subsp. hissarica (гиссарский подвид) и Yersinia pestis subsp. ulegeica (удэгейский подвид).
Заражение человека происходит через укус блох, при прямом контакте с заразным материалом, воздушно-капельным, редко алиментарным путем (например, при употреблении мяса верблюдов, больных чумой). В 1998-1999 гг. чумой в мире переболело 30 534 человека, из них 2 234 умерли.
, , , , , ,
Симптомы чумы
В зависимости от способа заражения различают бубонную, легочную, кишечную форму чумы; редко септическую и кожную (гнойные пузырьки на месте укуса блохи). Инкубационный период при чуме варьирует от нескольких часов до 9 сут. (у лиц, подвергнутых серопрофилактике, до 12 сут.). Возбудитель чумы проникает через мельчайшие повреждения кожи (укус блохи), иногда через слизистую оболочку или воздушно-капельным путем, достигает регионарных лимфатических узлов, в которых начинает бурно размножаться. Болезнь начинается внезапно: сильная головная боль, высокая температура с ознобом, лицо гиперемировано, затем оно темнеет, под глазами темные круги («черная смерть»). Бубон (увеличенный воспаленный лимфатический узел) появляется на второй день. Иногда чума развивается столь стремительно, что больной погибает раньше, чем появится бубон. Особенно тяжело протекает легочная чума. Она может возникнуть и как результат осложнения бубонной чумы, и при заражении воздушно-капельным путем. Болезнь развивается также очень бурно: озноб, высокая температура и уже в первые часы присоединяются боли в боку, кашель, вначале сухой, а потом с мокротой кровянистого характера; появляется бред, цианоз, коллапс, и наступает смерть. Больной легочной чумой представляет исключительную опасность для окружающих, так как выделяет с мокротой огромное количество возбудителя. В развитии болезни основную роль играет подавление активности фагоцитов: нейтрофильных лейкоцитов и макрофагов. Ничем не сдерживаемое размножение и распространение возбудителя через кровь по всему организму полностью подавляет иммунную систему и приводит (при отсутствии эффективного лечения) к гибели больного.
Лабораторная диагностика чумы
Используются бактериоскоиический, бактериологический, серологический и биологический методы, а также аллергическая проба с пестином (для ретроспективной диагностики). Материалом для исследования служат: пунктат из бубона (или его отделяемое), мокрота, кровь, при кишечной форме - испражнения. Yersinia pestis идентифицируют на основании морфологии, культуральных, биохимических признаков, пробы с чумным фагом и с помощью биологической пробы.
Простым и надежным методом определения антигенов чумной палочки в исследуемом материале является применение РПГА, особенно с использованием эритроцитарного диагностикума, сенсибилизированного моноклональными антителами к капсульному антигену, и ИФМ. Эти же реакции могут быть использованы для обнаружения антител в сыворотке больных.
Несмотря на наличие природных очагов, с 1930 г. на территории России в них не было ни одного случая заболевания людей чумой. Для специфической профилактики чумы используется прививка от чумы - живая ослабленная вакцина из штамма EV. Она вводится накожно, внутрикожно или подкожно. Кроме того, предложена сухая таблетированная вакцина для перорального применения. Поствакцинальный иммунитет формируется к 5-6-му дню после прививки и сохраняется в течение 11-12 мес. Для его оценки и ретроспективной диагностики чумы предложена внутрикожная аллергическая проба с пестином. Реакция считается положительной, если на месте введения пестина через 24-48 ч образуется уплотнение не менее 10 мм в диаметре и появляется краснота. Аллергическая проба положительна и у лиц, имеющих постинфекционный иммунитет.
Большой вклад в изучение чумы и организацию борьбы с ней внесли русские ученые: Д. С. Самойлович (первый не только в России, но и в Европе «охотник» за микробом чумы еще в XVIII в., он же первым предложил делать прививки против чумы), Д. К. Заболотный, Н. П. Клодницкий, И. А. Деминский (изучение природных очагов чумы, носителей возбудителя ее в очагах и т. п.) и др.
Важно знать!
Хорошо известно, как быстро могут распространяться инфекционные заболевания, - а значит, должны существовать и быть максимально доступными столь же оперативные способы детектирования инфекций буквально в полевых условиях, что критично в борьбе с эпидемиями.